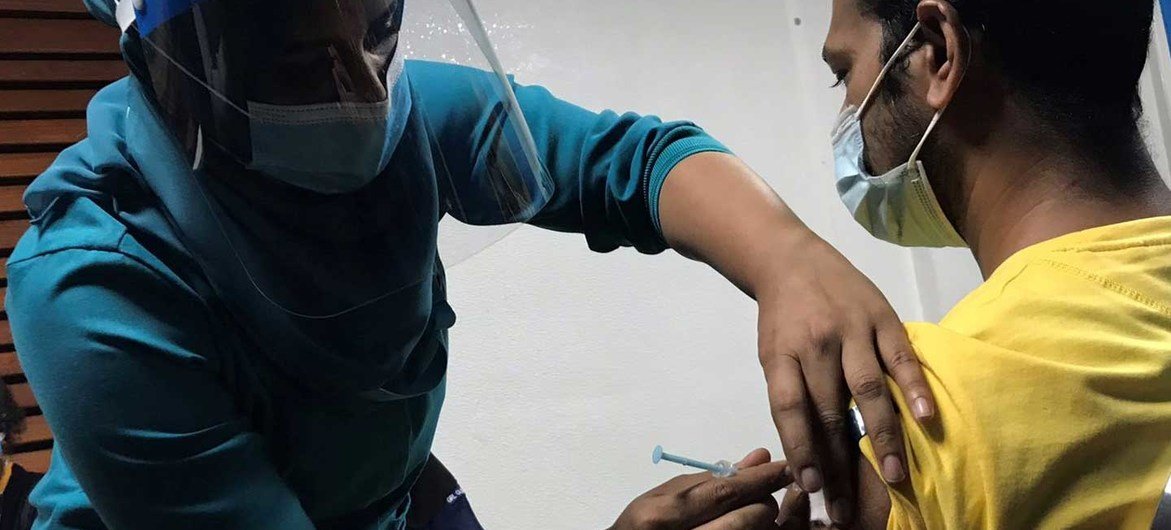
世卫组织:医保人员对宣传新冠疫苗安全性和有效性发挥着核心作用
声明表示,新冠大流行的全球影响使公众对疫苗的兴趣达到前所未有水平。但是,有关副作用的报道使一些人对接种疫苗表示担忧,延迟接种疫苗,甚至强烈反对接种疫苗。一些人对本国疫苗安全性监测系统的信心也存在差异。因此,清晰、一致的沟通宣传对于支持人们选择接种疫苗至关重要。
疫苗和监管程序
声明强调,监管机构严格评估疫苗厂商提供的科学和临床证据。监管机构还使用来自临床前实验室研究和人体临床试验的现有科学证据以及生产信息来评估候选疫苗的益处和风险。监管机构接下来会向独立的科学咨询委员会征求更多专家意见,以帮助决定是否批准疫苗。
全球公众可以对用于批准疫苗在更广泛人群中使用前科学评估疫苗安全性、有效性和质量的严格程序怀有信心。
潜在监管批准之前的安全性证据
声明表示,安全性证据是各种新冠疫苗提交监管审批的重要组成部分。公司向监管机构提交上市销售申请时,必须审查和报告所有不良事件。通常,监管机构将要求对临床试验参与者的随访必须至少持续到接种最后一剂疫苗之后1-2个月。根据以往经验,大多数不良事件发生在这样的时间范围内。
但是,有些罕见不良事件可能直到疫苗已在人群中广泛使用后才被发现。对于参与临床试验早期阶段的人员,还要进行更长时间的随访。监管机构会认真审查这些较长期试验的安全性数据,作为疫苗批准后安全性监测的一部分。
疫苗获批后的安全性和有效性监测
声明表示,疫苗获准使用后,监管机构将进行强有力的有效性监测,同时还要监测其安全性并开展降低风险活动。这需要持续监测疫苗安全性,以确保疫苗的益处继续超过风险。
此外,卫生保健专业人员不仅要及时地报告他们在患者身上看到的任何不良事件,而且鼓励已接种疫苗的人立即向卫生保健专业人员报告不良事件,或向有关国家的药品监管机构报告。
不幸的是,新冠疫苗的广泛使用,包括在老年人和有基础性疾病的患者中使用,意味着肯定会出现纯属巧合和与疫苗无关的死亡和严重疾病。每个监管机构以及相关医学专家和疫苗厂商将特别注意监测某些群体的安全,例如孕妇、本就患有严重疾病的人、老人、儿童以及为预防其他疾病接种了疫苗的人。
通常报告的不良事件
关于新冠疫苗,最常报告的事件是预期的疫苗副作用,如头痛、疲乏、肌肉和关节疼痛、发热、发冷和注射部位疼痛。这些不良事件的发生与临床试验中已知的疫苗情况一致。
特别关注的不良事件
过敏反应是任何疫苗都可能出现的非常罕见的副作用。其他一些不良事件包括面神经无力、惊厥、味觉丧失或小的心脏病事件,但没有一个被证实与疫苗有因果关系。
对使用信使核糖核酸(mRNA)疫苗(包括辉瑞疫苗和莫德纳疫苗)报告的特别令人关注的主要不良事件是过敏反应。监管机构仔细审查可能的过敏反应报告,以确定它们是否与真正的过敏反应一致,以及它们是否有可能是由疫苗引起的。过敏反应报告仍然非常罕见(大约每百万名接种者中有10例)。
其他一些不良事件包括异常出血和凝血障碍、面神经无力、惊厥、味觉或嗅觉丧失以及心脏病事件。监管机构监测并仔细审查疫苗与这些不良事件之间是否存在因果关系,在适当的情况下,这些事件将被纳入相关疫苗的产品信息/产品标签中。
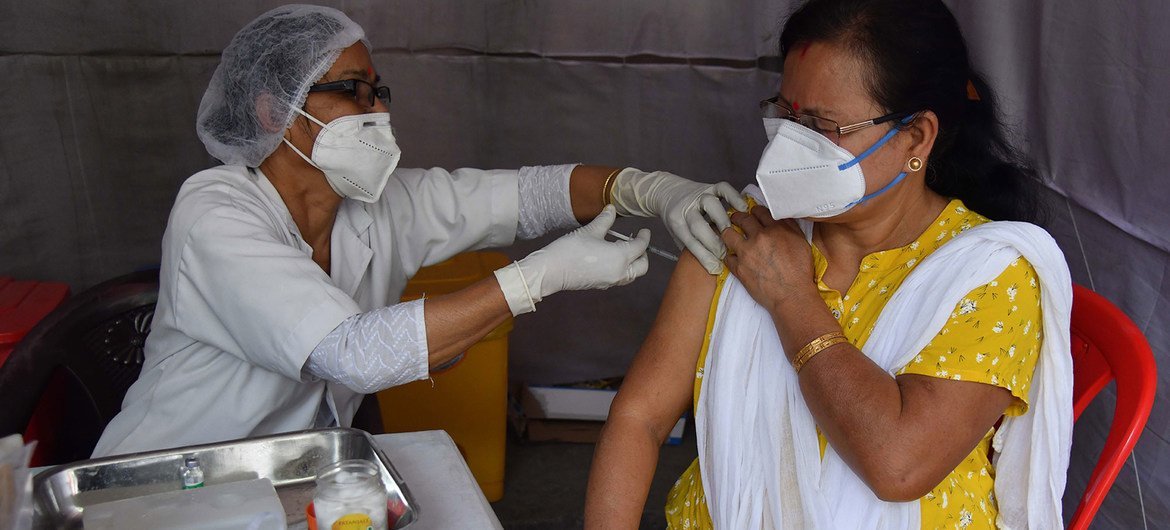
新冠疫苗有效期
声明表示,疫苗提供的保护持续时间可能有所不同。关键病毒蛋白的突变可能意味着病毒变体的出现。SARS-CoV-2冠状病毒容易发生突变,产生变体,其中一些变体已在世界许多地区形成。科学界和监管机构正在非常积极地监测现有疫苗是否能继续保护人们免受新变体的感染。
许多疫苗研发人员目前正在研发针对各种变体的疫苗,这些疫苗的强化注射可能会加强针对已知变体的保护作用。监管机构已同意,将根据对变体的免疫反应评估,促进对针对变体的疫苗数据的审查,就像每年评估新的季节性流感疫苗一样。