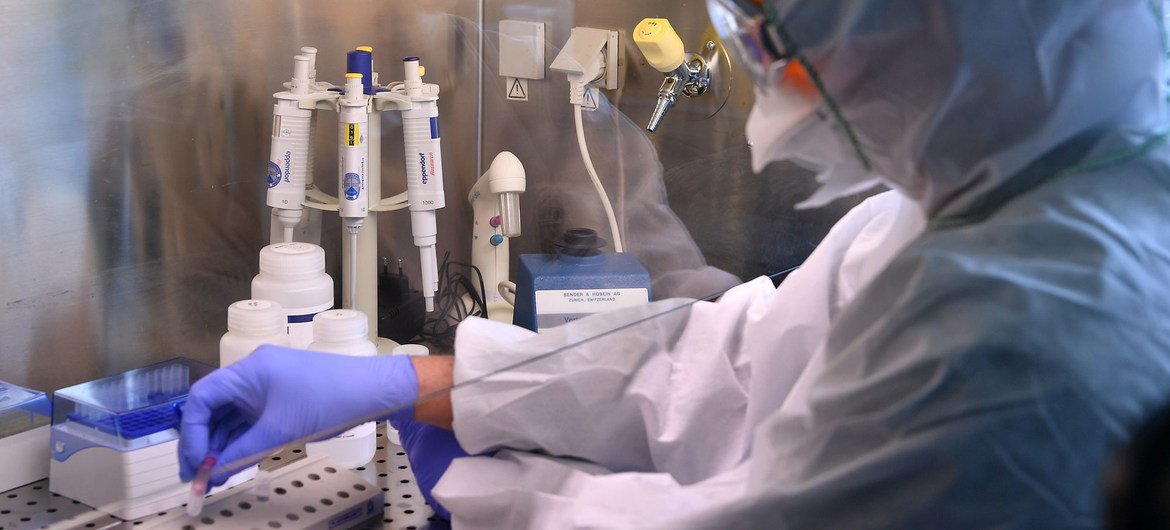
【专题报道】俄罗斯新冠疫苗“先声夺人” 有效性和安全性成为关注焦点
(普京同期声)
俄罗斯总统普京8月1日在与该国部长举行的视频会议上表示,在经过不到两个月的人体试验后,俄罗斯卫生部批准了该国自行研制的世界首支新冠疫苗。他表示,确保疫苗的安全和有效至关重要。他透露,自己的一个女儿也参加了疫苗接种实验。在第一次接种疫苗后,女儿出现了轻微的发烧。第二天体温降到了略高于正常的水平。第二次注射后又有点发烧,然后一切恢复正常。她目前感觉很好,抗体保持在很高的水平。
俄罗斯卫生部门表示,医务工作者、教师和其他高危人群将第一批接受疫苗注射,疫苗费用将由俄罗斯政府预算承担。
对于这一爆炸性的新闻,各国记者在当天联合国驻日内瓦办事处举行的例行记者会上纷纷请世界卫生组织的发言人就俄罗斯疫苗问题表态。
发言人贾萨雷维奇(Tarik Jasarevic)表示,加快疫苗开发的进展不能以牺牲疫苗的安全性和有效性为代价。他说,目前有160多种候选疫苗,世卫组织网站每周都在更新候选疫苗的概况。所有的标准都可以在世卫组织的网站上找到,所有候选疫苗都需要得到彻底审查。
贾萨雷维奇:“我们需要继续投资于加速研发安全有效的治疗手段和疫苗,以帮助减少病毒传播,但是加快进展不能、也不意味着在安全上做出妥协。加速疫苗的研发包括确保测试、制造和物流框架到位。世卫组织对任何疫苗的资格预审包括审查和评估通过临床试验收集的所有必需的有关安全性和有效性的数据。我们对几种候选疫苗的开发速度感到鼓舞,并希望其中一些将被证明是安全和有效的,并且通过疫苗共享机制,使其能够得到公平分配。”
俄罗斯将研制新冠疫苗的计划以1957年发射的世界第一个人造地球卫星“斯普特尼克一号”的名字命名,可见其想在疫苗的世界竞赛中拔得头筹的强烈愿望。为俄罗斯疫苗研发提供资金支持的俄罗斯主权财富基金的主席在接受美国有线电视新闻网的采访时直言不讳地将研发疫苗的竞赛同征服太空相比较。他说,当年美国在听到俄罗斯发射卫星的消息时大吃一惊,这次会是同样的一种情形。
在世界卫生组织于8月6日举行的例行记者会上,有记者问及俄罗斯准备在10月进行大范围接种新冠疫苗的计划是否让世卫组织感到担心时,世界卫生组织2019冠状病毒病遏制与治疗行动的负责人迈克尔·莱恩(Michael Ryan)没有对此正面回答,但在他所提及的目前受到世卫组织认可的六种进入第三阶段临床试验的候选疫苗当中没有包括俄罗斯的疫苗。
莱恩:“我们必须关注的是疫苗的加速开发,美国和世界上许多国家的许多人正在做大量的科学工作来加速疫苗的开发。现在有165种疫苗正处于研发阶段,26种在临床试验中,6种处于第三阶段试验中,这对于几个月的工作来说是一个不可思议的结果。我们现在需要做的是确保疫苗安全有效。这些研究正在进行,六种疫苗处于第三阶段试验,即针对大量志愿者展开实验。随着这项工作的继续,我们必须继续关注安全性和临床效果的信号。如果我们发现信号是积极的,我们将开始生产这种疫苗,并开始在更广泛的人群中使用,但我们仍将不得不保持谨慎,因为我们扩大了接种人数。只有当你给很多人接种疫苗时,疫苗的副作用才会变得明显。因此,即使我们开始在广泛的人群中接种疫苗,仍需要一个监测阶段。这里没有捷径。我想美国的许多专家,国家卫生研究院的负责人托尼·福奇和其他人都说过这种话。我们在考虑风险时,不应该关注等式一边的财务问题,而应当更多地考虑安全因素。”
疫苗从临床试验到上市大规模投入使用,需要经过三期或三个阶段临床试验的考验。一期临床试验重点是观察使用的安全性,主要是通过少数易感健康志愿者作为受试者,来确定人体对疫苗不同剂量的耐受,以及了解它初步安全性的结果。这一阶段一般人数规模相对较小,有数十人或100人左右。二期临床试验是扩大样本量和目标人群,目的是针对疫苗在人群中初步有效性与安全性的结果,进一步进行确认,且确定免疫程序和免疫剂量。这一阶段一般受试者要数百人,甚至更多。要真正确定疫苗的有效性则主要依靠三期临床试验。对于传染病,一般需要观察一个流行周期来确定它对易感人群的保护率。三期临床试验需要的样本量更大,规模都是好几千,有的甚至上万人。三期临床试验结束,才能得到疫苗可否批准上市的科学依据。
目前,在世卫组织正式登记在册进行开发的165种新冠疫苗中,有139种处于研发初期,26种进入临床测试阶段,其中中国的三种疫苗、美国的两种疫苗以及英国的一种疫苗进入了第三阶段试验。中国的三种疫苗使用灭活病毒,美国的是核酸疫苗,而英国的疫苗使用的是所谓的非复制病毒载体。
俄罗斯方面表示,他们的疫苗使用的是同英国疫苗一样的非复制病毒载体,这种疫苗通常更难测试并确保机体对感染的特异反应,因此临床研究阶段耗时更长。然而,俄罗斯称,疫苗研发工作进展顺利,加马列亚流行病与微生物学国家研究中心研制的疫苗已经结束临床试验并正式注册。此外,由俄罗斯国家病毒学和生物技术研究中心开发的另一种疫苗目前正在进行临床试验,还有另外至少两种疫苗今后两个月也将申请启动临床试验。
迈克尔·莱恩表示,第三阶段临床试验并不意味着马上会取得成功。第三阶段意味着这是第一次将这种疫苗用于普通人群,或者健康个体,以观察疫苗是否能保护他们免受自然感染。事实上,这只是开始。
莱恩:“到目前为止,所有的研究都围绕着安全性、免疫原性和确保疫苗在少数人身上产生免疫反应,并且不会产生会阻止疫苗进入试验的不利事件。从这个意义上说,它们是疫苗必须通过的那道大门。进入这扇门之后,便是一场真正的疫苗竞赛,届时将需要证明它可以在很长的一段时间内保护大量的人。我们希望更多的研究将进入这些试验。正在试验的候选疫苗所具备的多样性令人满意,一种是核酸疫苗,两种是非复制型病毒载体疫苗,三种是灭活病毒。因此,我们在许多不同的平台上,在观摩来自许多不同国家的一系列产品。但是我们将不得不等待,看看将产生怎样的结果。”
世卫组织发言人贾萨雷维奇在8月11日的记者会上表示,该组织与俄罗斯卫生当局保持着密切联系,并正在就世卫组织可能对俄罗斯疫苗进行的资格预审进行讨论。他重申:任何疫苗的资格预审都包括严格审查和评估所有必需的涉及安全性和有效性的相关数据。
李茂奇,联合国纽约总部报道。